Anthony Atala despre creşterea de organe
2,018,132 views |
Anthony Atala |
TEDMED 2009
• October 2009
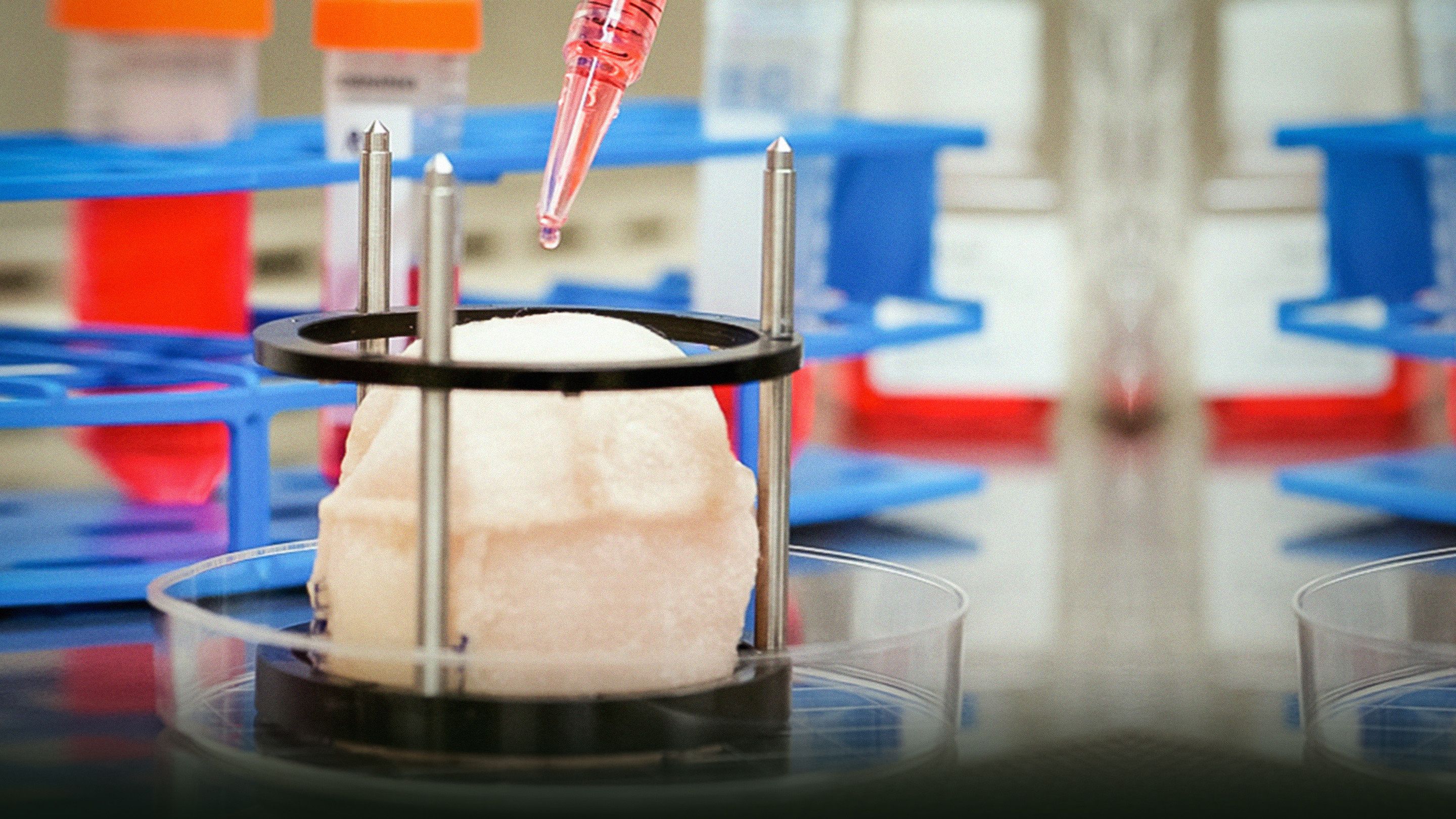
Laboratorul de ultimă generaţie al lui Anthony Atala produce organe pentru corpul uman -- de la muşchi până la vase de sânge, vezici şi altele. La TEDMED, ne arată materiale video ale bio-inginerilor săi lucrând cu aparate desprinse din domeniul ştiinţifico-fantastic, incluzând un bioreactor ca un cuptor (încălzit la 37ºC) şi o maşinărie care "tipăreşte" ţesut celular uman.